Por RT
Los resultados de la investigación permitiría a los investigadores comprender por qué algunos embriones fallan, mientras que otros culminan en un embarazo saludable.
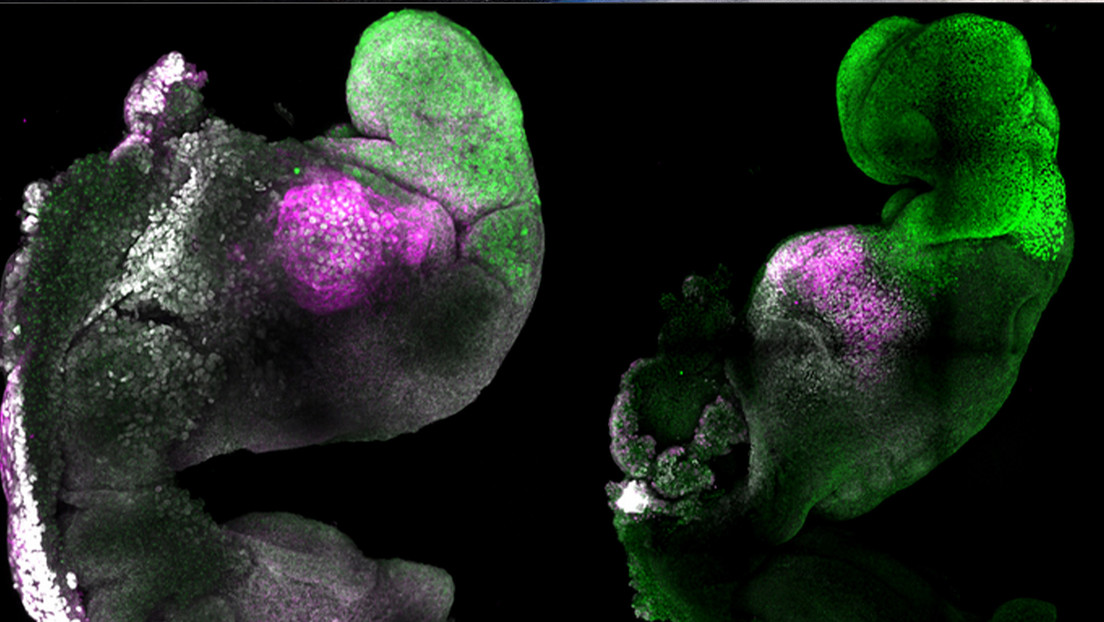
Para recrear las primeras etapas de la vida en mamíferos, investigadores de la Universidad de Cambridge, Reino Unido, han creado un modelo de embrión de ratón que forma un cerebro, un corazón que late y los cimientos de todos los demás órganos del cuerpo.
El equipo, dirigido por la profesora Magdalena Zernicka-Goetz, de manera novedosa desarrolló el embrión sintético sin óvulos ni espermatozoides. En su lugar, utilizó células madre, es decir, las partículas básicas del organismo que pueden convertirse en casi cualquier tipo celular.
Los investigadores imitaron los procesos naturales en el laboratorio guiando la interacción de los tres tipos de células madre que se encuentran en el desarrollo temprano de los mamíferos, mediante control genético. Lograron que estas transitaran por las sucesivas etapas de crecimiento embrionario hasta obtener corazones latiendo y cimientos de cerebro, o sea, hasta un nivel de avance nunca antes alcanzado por ningún otro modelo derivado de esta clase de células. Asimismo, desarrollaron el saco vitelino, donde el embrión crece y se nutre en sus primeras semanas.
«Nuestro modelo de embrión de ratón no solo desarrolla un cerebro, sino también un corazón que late, todos los componentes que forman el cuerpo», expresó Zernicka-Goetz en un comunicado de la universidad. «Es increíble que hayamos llegado tan lejos. Este ha sido el sueño de nuestra comunidad en años, y el principal enfoque de nuestro trabajo durante una década y finalmente lo hemos logrado», agregó.
Importancia del resultado
El equipo sostiene que estos resultados permitirían a los investigadores comprender por qué algunos embriones fallan, mientras que otros culminan en un embarazo saludable. Además, las conclusiones podrían usarse para guiar la reparación y la creación de órganos artificiales para trasplantes.
Asimismo, los investigadores creen que el modelo sintético de células madre es importante y novedoso porque posibilita acceder, para su estudio, a la estructura del diminuto embrión en una etapa en la que, normalmente, está oculto debido a la implantación en el útero de la madre. Esto permite manipular los genes para comprender sus funciones de desarrollo en un modelo experimental.
«Este período de la vida humana es muy misterioso, por lo que poder ver cómo sucede en una placa de Petri, tener acceso a estas células madre individuales, comprender por qué fracasan tantos embarazos y cómo podríamos evitar que eso suceda, es bastante especial«, sostuvo Zernicka-Goetz.
Otro elemento que los autores consideran significativo es que el desarrollo de estos embriones sintéticos abre nuevas posibilidades para estudiar los mecanismos del neurodesarrollo en un modelo experimental.
Actualmente, la legislación del Reino Unido permite estudiar embriones humanos en laboratorio hasta el día 14 de desarrollo, posibilitando a los investigadores elaborar modelos humanos similares con el objetivo de comprender qué mecanismos hay detrás de procesos cruciales que serían imposibles de analizar en embriones reales.
lo que permite que los investigadores desarrollen modelos humanos similares para comprender los mecanismos detrás de procesos cruciales que de otro modo serían imposibles de estudiar en embriones reales.
Proceso embrionario inicial
Para que un embrión humano crezca con éxito, debe existir comunicación entre sus tejidos y los que lo conectarán con la madre. En la primera semana posterior a la fertilización, se desarrollan tres tipos de células madre.
El primero se convertirá en los tejidos del cuerpo y los otros dos, extraembrionarios, apoyarán el desarrollo del feto. Uno se transformará en la placenta, que conecta al embrión con la madre y le proporciona oxígeno y nutrientes; mientras que el otro formará el saco vitelino, donde crece y se nutre durante el desarrollo temprano.
Los científicos publicaron los resultados de más de una década de investigación este jueves en la revista Nature.




Deja una respuesta